
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 [ 33 ] 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65
Реактор идеального смешения периодического действия. Уравнения, описывающие изотермический процесс в химическом реакторе периодического действия, совпадают с уравнениями (3.10) и (3.11), если в них условное время контакта реагентов заменить на время процесса t.
Устойчивость стационарньгх режимов химических реакторов. Стационарный режим работы реактора устойчив, если возникшее в некоторый момент времени малое возмущение параметра химического процесса (концентрации, температуры, давления и тд.) после устранения причины, вызывающей возмущение, постепенно исчезает и исходный стационарный режим работы восстанавливается. Если же отклонения от стационарного режима работы реактора увеличиваются во времени, то данный режим неустойчив.
Рассмотрим устойчивость стационарного адиабатического процесса в проточном реакторе идеального смещения. В этом случае отсутствует теплообмен с посторонним теплоносителем, и уравнения (3.7) и (3.8) преобразуются следующим образом;
(3.12)
гг(хд,7).
(3.13)
Пусть Хд(7) - решение уравнения (3.12), выражающее Хд как функцию Г при фиксированном т. Тогда в общем случае зависимость правой части уравнения (3.13) от температуры Гимеет вид кривой q (рис. 3.1).
Левая часть уравнения (3.13) - прямая и точки А, В, С пересечения и (7 определяют три стационарных режима. Физически это означает, что скорость тепловыделения q в результате реакции (правая часть уравнения (3.13)), равна скорости поглощения теплоты q при
Рис. 3.1. Зависимость тепловыделения q и теплоотвода от температуры Т. АиС-устойчивые режимы, В - неустойчивый режим
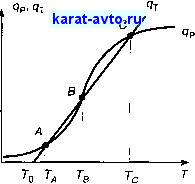
нафевании реагирующей смеси от исходной температуры до температуры Т, представленной левой частью уравнения (3.13), те. = 9.
Низкотемпературный режим А и высокотемпературный режим С являются устойчивыми, а промежуточный режим В неустойчив. Из рис. 3.1 видно, что для устойчивости стационарного режима необходимо, чтобы наклон прямой был больше наклона кривой в точке пересечения, те. скорость поглощения теплоты должна преобладать над скоростью тепловьщеления.
3.2.2. Примеры расчета
Пример 3.2-1. В реакторе идеального смешения объемом 0,3 м^ проводится экзотермическая реакция первого порядка К-К + Q. Константа скорости реакции, мин , описывается уравнением к = 103 ехр[-20000/(Л7)]. Тепловой эффект реакции составляет 9637 кДж/кмоль. Плотность реакционной массы не зависит от степени превращения и равна 420 кг/м^. Удельная теплоемкость раствора составляет 3,98 кДж/(кг-К). Раствор реагента А подается с концентрацией 6 кмоль/м^ в количестве 0,6 м^/ч.
Рассчитать, при какой температуре следует подавать исходный раствор компонента А в реактор, работающий в адиабатическом режиме, чтобы температура в нем не превышала 60 °С.
Решение. Находим константу скорости реакции при заданной температуре 333 К:
к = 103ехр[-20000/(8,31-333)] = 0,726 мин .
Согласно уравнению (3.9) можно определить температуру исходного раствора
Та=Т--4хд.
Для нахождения Хд воспользуемся формулой kz
~1 + кх
Определяем т как отношение объема реактора к объемному расходу реакционной смеси:
т = 0,3/0,6 = 0,5 ч = 30 мин
и находим
т т - AoQp
где
и, следовательно, степень превращения можно выразить как функцию температуры:
А = (7- Т,)/Т,- (а)
С другой стороны, для реактора смешения степень превращения тоже может быть выражена как некая функция температуры:
к(Т)т
Определяем АГ = 2,8-107-2,29Д2400-729) = 36,8 фад- Находим 1 = 50/1,75 = 28,6 с.
х,= =0,956
1 + 0,72-30
Определяем адиабатический разофев:
QpC 2300-6
А71 = -- =-= 34,6 град-
СрР 0,95-420
Определяем температуру исходной смеси:
Tq = Г- ДГадХд = 333 - 34,6-0,956 = 299,9 К.
Пример 3.2-2. Определить температуру проведения реакции и степень превращения, которые будут достигнуты, если реакцию А -> R + проводить в адиабатическом режиме в реакторе идеального смещения объемом 0,05 м^. Объемный расход реагента А с концентрацией 2,29 кмоль/м^ равен 1,75-10 mVc, константа скорости реакции, с~, описывается уравнением к = 1,310Зехр[-85300/(Л7)]. Тепловой эффект реакции равен 2,8-10 Дж/кмоль. Плотность реакционной смеси равна 729 кг/м^, а теплоемкость - 2400 ДжДкг-град) и не зависят от температуры. Температура входящего потока составляет 295 К.
Решение. При адиабатическом протекании процесса в реакторе существует связь между температурой и степенью превращения: